一、妊娠母体甲状腺激素变化的影响因素
(一)血清甲状腺素结合球蛋白(TBG)
甲状腺素结合球蛋白水平是影响妊娠母体甲状腺激素变化的主要因素之一。众所周知,甲状腺激素球蛋白的主要作用是在血中与甲状腺激素结合,将其运送至身体的各个组织。在血液中,甲状腺激素多以结合形式存在,游离状态极少;而在组织中发挥作用的则以游离甲状腺激素为主。
在妊娠期间,与雌激素增高趋势一致,血清TBG水平从妊娠6~10周开始逐渐升高,达到平台期后一直持续至妊娠结束,比妊娠初期可升高2-3倍。因此在妊娠期间,血清(结合)甲状腺激素水平也相应升高,一般而言,血清TT4水平可升高1.5~2倍,而组织中游离甲状腺激素(FT4、FT3)浓度可下降10~15%。
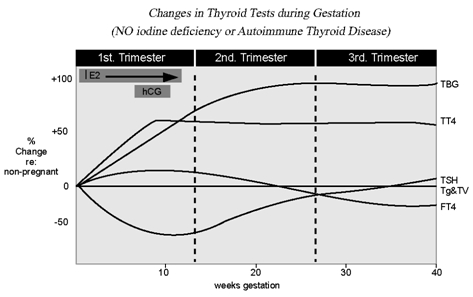
(二)血清绒毛膜促性腺激素(hCG)
从妊娠开始至妊娠12周左右,hCG水平也呈上升趋势,维持在较高水平,与FT4水平呈直线相关。此外,hCG与促甲状腺激素均来源于垂体,可竞争性结合甲状腺激素。在妊娠早期,由于hCG水平升高,因此血清游离甲状腺激素水平升高,而TSH则相应降低,两者变化呈镜像趋势。
(三)脱碘酶
脱碘酶的作用是使甲状腺激素脱碘,由T4转化成T3,或再由T3转化成T2,可分为I型、II型和III型。在妊娠期间,胎盘Ⅱ型、Ⅲ型脱碘酶活性增加,前者使T4转化成T3,后者使T4转化成rT3,而胎盘III型脱碘酶的相对活跃使其形成胎儿“低T3、高rT3”的甲状腺激素构成特点。
(四)肾脏对碘的清除率
在妊娠期间,肾脏对碘的清除力增强,因而母体对碘的需求量增加;而在妊娠中晚期,胎儿可通过胎盘从母体摄入碘,自行合成甲状腺激素,此过程也需要碘的参与;因此,在妊娠期间,母体若不及时补充碘的摄入,可能导致甲状腺激素不足,而形成甲状腺功能减低。WHO推荐妊娠妇女的碘摄入量不少于200 μg/日。
二、甲减分类
(一)根据病变发生的部位,可分为:
(1)原发性甲减(primary hypothyroidism):是指甲状腺腺体自身病变引起的甲减。此类甲减占全部甲减的95%以上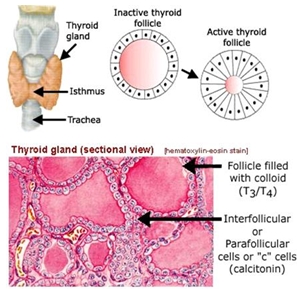 。原发性甲减的原因中自身免疫、甲状腺手术和甲亢131I治疗三大原因占90%以上。 。原发性甲减的原因中自身免疫、甲状腺手术和甲亢131I治疗三大原因占90%以上。
(2)中枢性甲减(central hypothyroidism):是指下丘脑和垂体病变引起的促甲状腺激素释放激素(TRH)或促甲状腺激素(TSH)产生和分泌减少引起的甲减。垂体外照射、垂体大腺瘤、颅咽管瘤及产后大出血是较常见原因。
(3)甲状腺激素抵抗综合征(resistance to thyroid hormones,RTH):是指甲状腺激素在外周组织实现生物效应障碍所引起的综合征。
(二)根据患病和诊断时期,可分为:
(1)妊娠前确诊甲减:即妊娠前即有甲状腺功能减退病史,并接受激素替代治疗,妊娠后由于药物剂量不足而再次出现甲减症状。
(2)妊娠期初确诊甲减:即妊娠前无甲低病史或未曾发现患病,妊娠后出现明显甲低症状,予以确诊,也称为“妊娠伴甲减”。
(三)根据临 床症状和激素水平,可分为: 床症状和激素水平,可分为:
(1)临床甲减:指患者具有甲低的临床症状,如怕冷、水肿、皮肤粗糙、便秘、精神差、嗜睡等,实验室检查发现TSH升高,TT4/FT4降低。
(2)亚临床甲减: 指患者没有甲低的临床症状或症状比较轻微,实验室检查显示TSH升高,TT4/FT4正常。
(3)低T4血症:是指既往无甲状腺病史,妊娠期间发现TT4/FT4降低,但TSH正常者,目前认为可能与碘有关。
|
 |
甲减的临床症状有哪些?妊娠期合并甲减对孕妇和胎儿有哪些危害?应如何诊断甲减? |
|
|
三、甲减临床表现
(一)低基础代谢率症群
主要表现为怕冷、少汗及体温低于正常。易疲乏,行动迟缓,嗜睡,记忆力减退,反应迟钝,注意力不集中。
(二)粘液性水肿面容
面部表情可以形容为“淡漠”,“假面具样”,“呆板”。面色苍白或蜡黄,面颊及眼睑虚肿,目光呆滞。鼻、唇增厚。舌大而发音不清,言语缓慢,音调低哑。头发干燥,稀疏,脆细,眉毛外1/3脱落,男性胡须生长缓慢。
(三)皮肤
患者因轻度贫血而苍白或因甲状腺激素缺乏导致高胡萝卜素血症,病人手脚皮肤呈姜黄色。全身皮肤干燥、粗糙、少光泽、易脱屑。水肿为非凹陷性,以颜面和下肢为主。指甲生长缓慢,厚脆,表面常有裂纹。腋毛和阴毛稀疏脱落。
(四)精神神经系统
反应迟钝,嗜睡,理解力和记忆力减退。有时可呈神经质,抑郁、失眠。可有手足麻木,痛觉异常。腱反射变化具有特征性,反射的收缩期往往敏捷,而松弛期延缓,跟腱反射减退,大于350毫微秒有利于诊断(正常为240-320ms)。膝反射多正常。
(五)肌肉和关节
患者肌肉松弛无力,主要累及肩、背部肌肉,常感肌肉疼痛、僵硬。关节也常疼痛,活动不灵,有强直感,受冷后加重。发育期间骨龄常延迟。骨质代谢缓慢,骨形成与吸收均减少。
(六)心血管系统
患者可出现脉搏缓慢,心动过缓,心音低弱,心输出量减低。由于心肌间质水肿、非特异性心肌纤维肿胀、左心室扩张和心包积液导致心脏增大。心包积液,经治疗后可恢复正常。10%患者伴有血压增高。久病者易并发动脉粥样硬化。冠心病发病率高于一般人群,由于组织耗氧量和心输出量的减低相平行,故心肌耗氧量减少,很少发生心绞痛和心力衰竭。心力衰竭,一旦发生,因洋地黄在体内的半衰期延长,且由于心肌有粘液性水肿故常常疗效不佳且易发生洋地黄中毒。心绞痛在经左甲状腺素治疗后可加重。ECG显示低电压,T波倒置,QRS波增宽,P-R间期延长,个别患者可出现心肌梗塞的心电图表现。SGOT、LDH及CPK可增高,经治疗后均可消失。心肌纤维肿胀,有PAS染色阳性的粘液性糖蛋白沉积以及间质纤维化,称甲减性心肌病变。
四、母体甲减对妊娠和胎儿的影响
(一)母体甲减对妊娠的影响
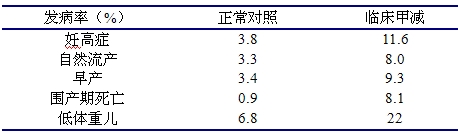
如果在妊娠期出现甲减,对妊娠过程将产生显著影响,如妊高症、流产、早产、围产期死亡等,其发生率明显升高,相关研究的数据如下表所示:
发病率(%) |
正常对照 |
临床甲减 |
妊高症 |
3.8 |
11.6 |
自然流产 |
3.3 |
8.0 |
早产 |
3.4 |
9.3 |
围产期死亡 |
0.9 |
8.1 |
低体重儿 |
6.8 |
22 |
临床甲减比亚临床甲减发生上述并发症的危险更大,而亚临床甲减妊娠并发症的危险性是否升高结论不一,但多数仍认为有一定影响。
(二)母体甲减对后代智力的影响
一项关于母体甲减对后代智力影响的回顾性分析对62名甲减孕妇和124名正常孕妇进行了比较。在妊娠17周时,甲减孕妇的TSH值显著高于正常孕妇,而TT4和FT4水平则显著降低。与之相应,抗甲状腺球蛋白抗体和抗甲状腺过氧化酶抗体也明显升高,提示患者具有甲状腺自身免疫性倾向。然后,采用韦氏儿童智力量表测定7-9岁儿童的智商。在124名孕妇对照组中,后代智商分值是107±12,48名未治疗甲减孕妇的后代智商分值是100,14名已治疗甲减孕妇的后代智商分值是111。
由此可见,妊娠妇女若未诊治甲减,将对后代神经发育产生不良影响。如果对妊娠合并甲减患者给予L-T4治疗,儿童智力将不被影响。
此外,另一项研究对甲减和正常孕妇组进行比较,评价其1岁和2岁孩子的智力发育和运动能力,结果发现在妊娠12周时母体低T4血症(血清FT4低下,TSH 正常(0.15-2.0 mIU/L)),其后代在1岁、2岁时的智力发育和运动能力评分均低于正常对照组。
|
病例 |
对照 |
P值 |
1岁 |
|
|
|
智力发育 |
95 |
105 |
0.004 |
运动能力 |
91 |
99 |
0.02 |
2岁 |
|
|
|
智力发育 |
98 |
106 |
0.02 |
运动能力 |
92 |
102 |
0.005 |
五、实验室检查
血清促甲状腺激素(TSH)和TT4和FT4是甲减的第一线指标。原发性甲减血清TSH增高,TT4和FT4均降低。TSH增高,TT4和FT4降低的水平与病情程度相关。血清TT3、FT3早期正常,晚期减低。因为T3主要来源于外周组织T4的转换,所以不作为诊断原发性甲减的必备指标。亚临床甲减仅有TSH增高,TT4和FT4正常。
|
病例 |
对照 |
P值 |
1岁 |
|
|
|
智力发育 |
95 |
105 |
0.004 |
运动能力 |
91 |
99 |
0.02 |
2岁 |
|
|
|
智力发育 |
98 |
106 |
0.02 |
运动能力 |
92 |
102 |
0.005 |
甲状腺过氧化物酶抗体(TPOAb)、甲状腺球蛋白抗体(TgAb)是确定原发性甲减病因的重要指标和诊断自身免疫甲状腺炎(包括桥本甲状腺炎、萎缩性甲状腺炎)的主要指标。一般认为TPOAb的意义较为肯定。日本学者经甲状腺细针穿刺细胞学检查证实,TPOAb阳性者的甲状腺均有淋巴细胞浸润。如果TPOAb阳性伴血清TSH水 平增高,说明甲状腺细胞已经发生损伤。我国学者经过对甲状腺抗体阳性,甲状腺功能正常的个体随访五年发现:当初访时TPOAb>50IU/ml和TgAb>40IU/ml,临床甲减和亚临床甲减的发生率显著增加。 平增高,说明甲状腺细胞已经发生损伤。我国学者经过对甲状腺抗体阳性,甲状腺功能正常的个体随访五年发现:当初访时TPOAb>50IU/ml和TgAb>40IU/ml,临床甲减和亚临床甲减的发生率显著增加。
(一)血清TSH在诊断中的应用
在临床诊断中,目前尚缺乏孕期特异性TSH参考范围。一般而言,妊娠早期TSH参考范围应低于非妊娠人群30-50%,而正常人的TSH参考范围是0.5-5.0 mIU/L。此外,有部分学者提出2.5 mIU/L作为妊娠早期TSH正常范围的上限。
(二)血清TT4/FT4在诊断中的应用
TT4/FT4在诊断甲低中也非常重要,但目前尚无孕期特异性的TT4/FT4参考范围。由于FT4波动较大,受检测方法影响,不推荐使用,而TT4浓度增加稳定,约为非妊娠时的1.5倍。国际上推荐应用TT4评估妊娠期的甲状腺功能。如果TSH正常(0.3-2.5 mIU/L),TT4低于100 nmol/L(7.8 μg/dL),可诊断为妊娠低T4血症。
|
 |
L-T4(左甲状腺素钠)是目前临床上应用最为广泛的甲状腺激素替代治疗用药,那么L-T4治疗的目标是什么?应如何调整剂量?注意事项有哪些? |
|
|
六、治疗、筛查和预防
(一)治疗
L-T4(左甲状腺素钠)是治疗甲减的首选替代治疗药物。如果在妊娠前确诊甲减,则应调整L-T4剂量,待TSH正常后再怀孕;如果在妊娠期才确诊甲减,则L-T4剂量应较非妊娠时增加30%-50%,且一经诊断,立即治疗,可给予L -T4 2.0 μg/kg/d,并依据妊娠特异的TSH正常范围,调整L-T4剂量。有学者建议TSH 2.5 mIU/L作为补充L-T4的目标值。在调整L-T4剂量期间,应每2-4周测定一次TSH。越早达标(最好在妊娠8周之内),越有利于控制病情,减少对后代的智力影响。TSH达标以后,每6-8周监测一次TSH、FT4和TT4。 -T4 2.0 μg/kg/d,并依据妊娠特异的TSH正常范围,调整L-T4剂量。有学者建议TSH 2.5 mIU/L作为补充L-T4的目标值。在调整L-T4剂量期间,应每2-4周测定一次TSH。越早达标(最好在妊娠8周之内),越有利于控制病情,减少对后代的智力影响。TSH达标以后,每6-8周监测一次TSH、FT4和TT4。
对于亚临床甲减的妊娠妇女,是否治疗目前尚无一致意见,但多数学者认为有必要治疗。
L-T4应当空腹服用,并避免与离子补充剂一起使用,因为后者含有很多微量元素,可能影响L-T4的吸收和利用度。对于钙剂和黄豆等食品等的摄入,应间隔4小时以上。
(二)筛查
对于妊娠妇女是否应做TSH常规筛查,目前医学界意见尚不统一。美国医学会(AACE)认为,鉴于甲减和轻度甲减对于后代的危害,所有妇女在怀孕后应立即筛查甲状腺TSH;而美国甲状腺协会(ATA)认为,目前尚缺乏大规模前瞻性研究结果,目前全面筛查为时尚早。
(三)预防
现在一致认为,对于甲减高危人群,应进行妊娠前甲状腺功能筛查。甲状腺高危人群包括:
1. 有甲状腺疾病个人史和家族史者;
2. 有甲状腺肿和甲状腺手术切除和131I治疗史者;
3. 既往发现血清TSH增高或甲状腺自身抗体阳性者;
4. 有其他自身免疫性疾病个人史和家族史者。
七、妊娠与甲状腺功能亢进症
(一)病因
妊娠合并甲状腺功能亢进可分为两种:
1. 妊娠一过性甲状腺毒症(gestational transient thyrotoxicosis,GTT):常在妊娠前三个月发生,是一种hCG相关性甲亢,hCG增高的水平与病情程度相关,无自身免疫性甲状腺疾病史,TRAb及TPOAb阴性,甲状腺功能的改变多为暂时性。临床上主要表现为妊娠剧吐,一过性甲亢(THHG),伴剧烈恶心、呕吐,体重下降5%以上,严重时出现脱水和酮症,是妊娠早期甲亢最常见的原因。由于hCG主要在妊娠早期维持高水平,因此这种甲亢仅为一过性,可自行缓解,一般无需治疗。
2. 妊娠Graves病:与甲状腺自身免疫异常有关,由甲状腺自身免疫功能紊乱所致。
(二)诊断与鉴别诊断
1. 疑诊甲亢:一般而言,若孕妇体重不随妊娠月数而相应增加,或四肢近端肌肉消瘦,或休息时心率在100次/分,应考虑甲亢可能性。
2. 确诊甲亢:在疑诊甲亢时,如果实验室检查显示血清TSH<0.3 mIU/L,T3或T4升高,则可确诊甲亢。
3. 鉴别甲亢原因:在确诊甲亢后,应进一步鉴别甲亢原因,为后续治疗提供依据。对于GTT,鉴于此病仅为一过性,可自行缓解,一般给予对症处理即可,如止吐、输液和不同营养物质。对于妊娠Graves病,临床上表现为妊娠前5个月症状逐渐加重,后5个月症状可能减轻,此时应谨慎处理,进行抗甲状腺药物治疗。
|
 |
如果在妊娠期合并甲亢,对母体和胎儿会产生哪些危害呢? |
|
|
(三)妊娠期甲亢的危害
1. 对母体的危害:如妊高症、先兆子痫、心力衰竭,严重者可出现甲状腺危象、流产和胎盘早剥。
2. 对胎儿的危害:包括宫内生长停滞、早产儿、死胎、先天畸形和新生儿死亡等。此外,足月小样儿的发生率是正常妊娠妇女的9倍,GD孕妇中新生儿甲亢患病率可达1-2%。
下表所示为342例甲亢患者的妊娠结果:
|
ATD治疗组 |
手术治疗组 |
未治疗组 |
总样本数 |
265 |
43 |
34 |
死胎 |
12(5%) |
3(7%) |
8(24%) |
早产 |
29(11%) |
4(9%) |
18(53%) |
发育异常 |
3(1%) |
1(2%) |
|
甲状腺危象 |
5(2%) |
1(2%) |
7(21%) |
以上数据显示,未治疗组的死胎、早产和甲状腺危象的发病率较治疗组升高,经治疗控制甲亢上述疾病的发生率降低。
(四)妊娠期甲亢的治疗
甲亢的治疗有三种:(1)抗甲状腺药物治疗:是治疗妊娠期甲亢的首选,一般选在妊娠中期(即妊娠4~6个月时);(2)手术治疗:应选择合适的时机;(3)放射性131I治疗:是妊娠期甲亢治疗的绝对禁忌,因为放射性碘可通过胎盘影响胎儿的生长和发育。
1.手术
对于妊娠期甲亢,若进行手术治疗,应选在妊娠4~6个月为宜,其手术适应证有:
①对抗甲药过敏者;
②抗甲药治疗效果不佳,或不能规律服药者;
③甲状腺肿显著,需要大剂量ATD者;
④心理负担重,过度担心药物副作用者;
2. 抗甲状腺药物
抗甲状腺药物的首选是丙硫氧嘧啶,二线药物是甲巯咪唑。如下表所示,甲巯咪唑的胎儿/母体药物浓度是丙硫氧嘧啶的2~3倍,其胎盘通过率也高于丙硫氧嘧啶,两者的先天性畸形发生率相似。关于胚胎发育不良,丙硫氧嘧啶尚无确切报告,而甲巯咪唑显示可能导致胎儿先天性皮肤缺损、气管食管瘘或面部畸形等,鉴于以上原因,丙硫氧嘧啶成为妊娠甲亢药物治疗的一线用药。
|
丙硫氧嘧啶 |
甲巯咪唑 |
胎儿/母体药物浓度比 |
0.27-0.35 |
0.72-1.0 |
胎盘通过率 |
低 |
较高 |
先天畸形发生率 |
3% |
2.7% |
胚胎发育不良 |
|
先天性皮肤缺损
气管-食管瘘
面部畸形等 |
药物选择 |
优先 |
第二线药物 |
3. 妊娠期抗甲状腺药物(ATD)的应用
丙硫氧嘧啶(PTU)的最大剂量是50-100mg,q8h,而甲巯咪唑(MMI)则为20mg/天。一般而言,在治疗初期每2周检查一次甲状腺功能,以后可延长至2~4周一次。当临床症状和甲状腺功能逐渐改善时,ATD的剂量应逐渐减量。多数患者在用药3-8周后甲功恢复正常,当患者依赖最小剂量的ATD(PTU 50mg/天或MMI 5mg/天)维持甲功正常持续数周后,可以停药。目前主张维持治疗至妊娠32周,避免甲亢复发。如果复发可以再次用ATD治疗。
4. 治疗目标
治疗目标是用尽量少的ATD剂量,尽快有效控制甲亢症状,尽早使甲状腺功能恢复正常,血清FT4 在正常值的上1/3范围,而TSH水平不能作为甲亢治疗时的监测指标。总体上而言,治疗应保证母亲和胎儿无并发症发生。
5. ATD与其他药物的联合使用
(1)ATD与LT4联合使用:联合L-T4用药后,ATD控制甲亢的剂量需要增加,因此妊娠期甲亢一般不建议联合使用L-T4。
(2)β受体阻断剂的应用:有研究表明,普奈洛尔(心得安)与自发性流产有关,患病率为24.4%(正常人5.5%),可能引起胎儿宫内生长迟缓、产程延长、新生儿心动过缓、低血压等并发症,故应慎重使用。
6. 抗甲状腺药物与哺乳
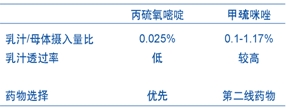
哺乳期使用PTU 150mg/天或MMI 10mg/天对婴儿脑发育没有显著影响,但仍应监测婴儿的甲状腺功能。哺乳完毕后可服用ATD,需间隔3-4小时再行下一次哺乳。
7. 甲亢患者妊娠时机
对于既往患甲亢者,若在ATD治疗期间,血清TSH达正常范围,停用ATD或减少ATD剂量后,血清FT4处于正常值上限,则可试行怀孕。部分学者主张怀孕前应当停用MMI,改为PTU治疗,以避免MMI可能引起的后代畸形。此外,在甲亢放射碘治疗后6个月内应避免怀孕,尽管目前尚无证据证实放射性碘对胎儿及后代的负作用。
|